
Medizinprodukte finden Verwendung in der Diagnostik, Prävention und Behandlung von Krankheiten. In der Medizin unterscheidet man zwischen verschiedenen Klassen von Produkten, die anhand ihres Risikos bei der Verwendung eingeteilt werden. Für die Zulassung solcher medizinischen Ausrüstung braucht es Fachübersetzungen, da die Sicherheitshinweise und Betriebsanleitungen in der jeweiligen Landessprache vorliegen müssen. Wir sind das passende Übersetzungsbüro für diese wichtige Aufgabe!
Medizinprodukte: Eine Definition
Unter dem Begriff Medizinprodukt fasst man unter anderem medizinische Instrumente, Implantate und Softwares zusammen. Sie werden für die Behandlung, Erkennung und Vorbeugung von Krankheiten genutzt. Im Unterschied zu Arzneimitteln wirken Medizinprodukte dabei physisch. Arzneien setzen ihre Wirkung hingegen auf chemischem Weg, also metabolisch, immunologisch oder physiologisch frei.
Bedeutung von Medizinprodukten
Medizinprodukte sind sowohl für das Gesundheitswesen als auch für die Wirtschaft von großer Bedeutung. Im Gesundheitswesen verbessern sie dabei stetig die Diagnose- sowie Behandlungsmöglichkeiten und steigern die Lebensqualität zahlreicher Menschen. Für die Wirtschaft sind sie nicht weniger bedeutend. Denn im weltweiten Ranking ist der deutsche Markt der drittgrößte in diesem Bereich. Im Jahr 2021 lag der Gesamtumsatz in der Medizintechnik beispielsweise bei mehr als 36 Mrd. € und steigt im Vergleich zu Vorjahren immer weiter an.
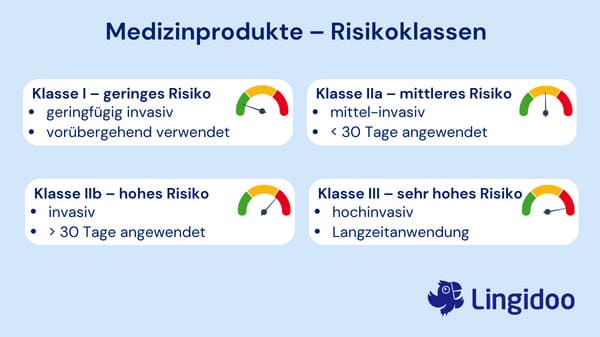
Risikoklassen für Medizinprodukte
Medizinische Produkte kann man anhand des Risikos bei der Anwendung in Risikoklassen einteilen. Diese haben einen Einfluss darauf, welche regulatorischen Anforderungen für die Zulassung existieren. Von dieser Klassifizierung ausgenommen sind laut der IHK Pfalz lediglich die sogenannten In-Vitro-Diagnostika. Es gibt dabei vier unterschiedliche Risikoklassen nach der EU-Medizinprodukteverordnung (MDR). Für die Einteilung spielen unter anderem die Länge der Anwendung und der Anwendungsort eine Rolle.
Klasse I
Sie stellen ein niedriges Risiko für die Patientinnen und Patienten dar und sind nicht invasiv. Außerdem werden sie nur vorübergehend angewendet. Solche Medizinprodukte sind zum Beispiel Stethoskope, Verbandsmaterial oder Gehhilfen.
Klasse IIa
Bei dieser Klasse besteht ein mittleres Risiko und sie sind mäßig invasiv. Solche Produkte werden zudem nur für eine kurze Zeit (weniger als 30 Tage) angewendet. Beispiele sind der Ultraschall oder Kontaktlinsen.
Klasse IIb
Hierunter versteht man medizinische Produkte, die ein höheres Risiko bergen und systemisch wirken. Sie haben also einen Einfluss auf den gesamten Organismus und sind überdies für eine Langzeitnutzung (länger als 30 Tage) ausgelegt. Darunter zählt man Beatmungsgeräte, Dialysatoren und Röntgengeräte.
Klasse III
Für diese Kategorie gilt ein hohes Risiko, denn sie werden implantiert und sind für eine Langzeitanwendung bestimmt. Hierzu werden etwa Prothesen, Implantate sowie Stents gezählt.
Einteilung anhand des Infektionsrisikos
Abhängig vom Anwendungsbereich eines Produktes ergeben sich überdies unterschiedliche Anforderungen an die Reinigung bzw. Sterilisation bei einer Wiederverwendung. Daher gibt es noch eine zweite Klassifizierungsmöglichkeit, die sich auf das Risiko einer Infektionsübertragung bezieht. Man unterteilt dann wie folgt in unkritische, semikritische und kritische Medizinprodukte:
Tabelle 1: Einteilung von Medizinprodukten nach Infektionsrisiko
| Einteilung | Erklärung | Aufbereitung | Beispiel |
| Unkritisch | Kein direkter Kontakt mit den behandelten Personen oder nur mit unversehrter Haut. | Reinigung + Desinfektion | Blutdruckmanschetten, Stethoskope |
| Semikritisch | Kommen mit nicht intakter Haut oder Schleimhäuten in Kontakt. Unterteilt in A und B. | A: ohne erhöhte Anforderungen; B: erhöhte Anforderungen | A: Verbandscheren, Mundspiegel; B: Beatmungsmasken, Narkoseschläuche |
| Kritisch | Dringen durch die Haut in Gewebe und Blutkreislauf ein. Unterteilt in A, B und C. | A: keine besonderen Anforderungen; B: höhere Anforderungen; C: Sehr hohe Anforderungen | A: Klemmen, Scheren; B: Sauger, MIC Instrumente; C: Angioskope, ERCP-Katheter |
Regulation von medizinischen Produkten
Für Medizinprodukte existieren strenge Maßnahmen zur Qualitätssicherung, die die Patientensicherheit sowie die Sicherheit der anwendenden Fachpersonen gewährleisten sollen. Werden Geräte wie Blutdruckmessgeräte direkt von Fachfremden angewendet, sind überdies verständliche Patienteninformationen in Form von Gebrauchsanweisungen oder Sicherheitshinweisen nötig. Die entsprechenden Anforderungen an die Produkte und die Hersteller:innen sind durch die EU-Medizinprodukteverordnung (MDR) sowie die Verordnung über In-vitro-Diagnostika (IVDR) festgelegt. Die Erfüllung dieser Anforderungen ist für die Zulassung nötig und wird durch die CE-Kennzeichnung bestätigt.
Zu medizinischen Produkten zählt man eine Vielzahl von Instrumenten, Geräten sowie Softwares, die in der Medizin etwa bei der Diagnose oder Behandlung zum Einsatz kommen. Diese Produkte werden von Herstellerinnen und Herstellern international betrieben und unterliegen strengen Richtlinien. Es wird beispielsweise verlangt, alle für eine sichere Verwendung nötigen Informationen in der jeweiligen Landessprache zur Verfügung zu stellen. Daher sind Übersetzungen ins Englische und viele weitere Sprachen nötig. Wir übernehmen diese Aufgabe mit größter Expertise – auch im Express.
FAQs zu Medizinprodukten
Dazu zählen laut Definition alle Produkte, die in einem medizinischen Rahmen für die Behandlung von Menschen verwendet werden. Neben Implantaten oder ärztlichen Instrumenten sowie medizinischen Geräten fallen darunter selbst Verbandsmaterial oder Softwares. Die Ergebnisse der dank ihnen gewonnenen Erkenntnisse werden für die medizinische Dokumentation und Weitergabe von Informationen dann wiederum in Arztbriefen festgehalten. Sie selbst sind jedoch kein Medizinprodukt.
Nein, Arzneimittel gehören nicht zu den medizinischen Produkten. Denn diese wirken physikalisch, während Arzneimittel den Metabolismus, die Physiologie oder das Immunsystem beeinflussen.
Nicht dazugezählt werden etwa Arzneimittel oder Softwares, die nicht für spezifische medizinische Zwecke eingesetzt werden sollen.
Einige Beispiele sind Katheter, Infusionen, Rollstühle, Produkte aus der Zahnmedizin sowie Stethoskope. Es gibt demnach eine große Bandbreite verschiedenster Instrumente und Geräte.
Wenn ein Produkt alle in der MDR oder der IVDR definierten Anforderungen für die Zulassung erfüllt, dürfen Hersteller:innen eine CE-Kennzeichnung vornehmen. Ist ein Produkt einer höheren Risikoklasse zugeordnet, muss zusätzlich eine sogenannte Benannte Stelle für die Prüfung beauftragt werden.


